Microbioma cutaneo e acne: nuova frontiera 2026

La lotta contro l'acne sta cambiando radicalmente direzione.
Dimentica per un momento la guerra totale contro i batteri: la scienza del 2026 ci rivela che il segreto per una pelle libera da imperfezioni non risiede nell'eliminazione indiscriminata dei microrganismi, bensì nel loro equilibrio.
Il microbioma cutaneo - complessa comunità di batteri, funghi, virus e acari che abita la nostra pelle - si sta rivelando il protagonista nella genesi e nel trattamento dell'acne vulgaris.
Scopriamo insieme come la comprensione di tale ecosistema invisibile stia aprendo porte verso terapie più intelligenti ed efficaci.
L'ecosistema nascosto della nostra pelle
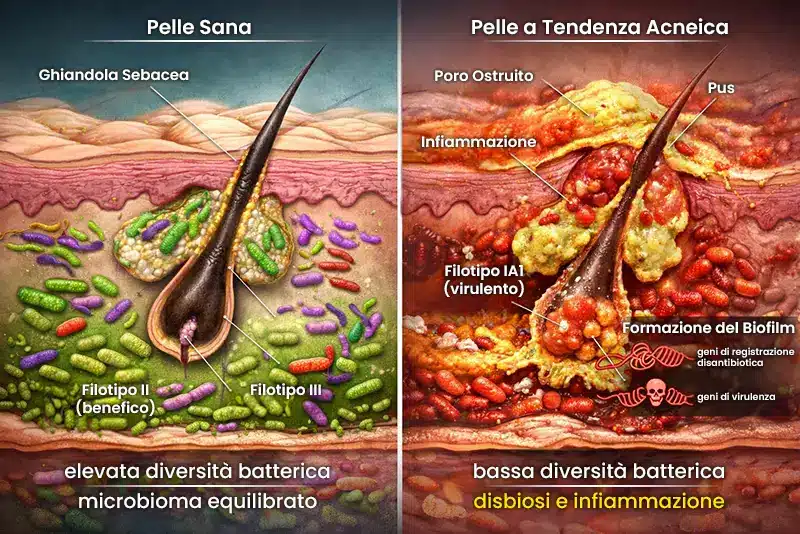
La pelle ospita circa mille miliardi di batteri, un numero impressionante seppur dieci volte inferiore rispetto ai microrganismi intestinali [1]. Tali abitanti microscopici non sono semplici inquilini passivi: formano un ecosistema dinamico in costante dialogo con il nostro sistema immunitario.
Il microbiota cutaneo - termine che indica l'insieme dei microrganismi - differisce significativamente in base alle diverse zone del corpo. Le aree sebacee quali viso, torace e schiena sono dominate dal genere Cutibacterium, mentre la maggior parte della superficie cutanea presenta maggiore presenza di Staphylococcus e Corynebacterium [2].
Quando parliamo di microbioma, ci riferiamo non solo alla comunità microbica in sé, nel dettaglio al suo patrimonio genetico complessivo e alle interazioni con l'ambiente circostante.
La distinzione è importante: mentre il microbiota cambia costantemente, il microbioma ci fornisce informazioni più stabili sulle capacità funzionali di tale ecosistema. In condizioni di salute, esiste uno stato di eubiosi - un equilibrio armonioso tra le diverse specie microbiche. Quando tale equilibrio si rompe, si instaura la disbiosi, aprendo la strada a condizioni patologiche tra cui l'acne.
Immagina di avere un orto pieno di piante diverse.
- Il microbiota ci dice quali piante ci sono nell’orto e quante sono. È soggetto a continue variazioni: una pianta cresce, un’altra muore, arriva un’erbaccia, ecc;
- Il microbioma ci indica cosa quell’orto è in grado di fare: ad esempio se può produrre frutta, se attira insetti utili, se mantiene il terreno sano; sono caratteristiche più stabili.
Quando l’orto è ben curato e le piante convivono bene, c’è equilibrio (eubiosi).
Se invece qualcosa va storto (troppa acqua, parassiti, erbacee…), le piante si sbilanciano e l’orto si rovina (disbiosi), possono comparire problemi, nel caso in esame, l’acne.
Cutibacterium acnes
Per decenni, Cutibacterium acnes (precedentemente Propionibacterium acnes) è stato considerato il principale colpevole dell'acne. Tale batterio Gram-positivo anaerobico risiede prevalentemente nei follicoli sebacei, nutrendosi del sebo prodotto dalle ghiandole.
Attraverso enzimi lipasi, degrada i trigliceridi del sebo in acidi grassi a catena corta, contribuendo al mantenimento del pH acido della pelle - normalmente una difesa contro patogeni pericolosi.
Gli studi hanno identificato sei filotipi distinti di C. acnes, con virulenza e comportamenti radicalmente diversi [3]. I filotipi IA e III contengono i ceppi più virulenti associati all'acne, mentre il filotipo II agisce da batterio benefico, preservando l'equilibrio del microbiota follicolare e prevenendo la colonizzazione da parte di ceppi patogeni. Uno studio italiano pubblicato su Scientific Reports ha individuato nel filotipo IA1 il ceppo più problematico: è capace di formare biofilm resistenti, mostra elevata tolleranza agli antibiotici e trasporta cassette di geni virulenti nel suo genoma [4]. Il filotipo IA1 è particolarmente associato alle forme più profonde e resistenti, quali l'acne cistica, dove il biofilm protegge i batteri dall'azione degli antibiotici.
La pelle sana presenta maggiore diversità di ceppi di C. acnes, con predominanza del filotipo II. La pelle acneica, al contrario, mostra una perdita di diversità batterica accompagnata dalla proliferazione del filotipo IA1. Non è la quantità totale di C. acnes a determinare l'acne, bensì lo squilibrio tra i vari filotipi. Tale meccanismo spiega perché individui sani possono ospitare abbondanti colonie di C. acnes senza sviluppare lesioni infiammatorie.
L'asse IGF-1 ha una funzione determinante anche nell'acne tardiva che colpisce gli adulti, dove dieta e stress amplificano la risposta infiammatoria.
La complessa rete di interazioni microbiche
Il microbioma cutaneo non è una collezione di singoli batteri: funziona attraverso un ecosistema interconnesso dove le specie competono, collaborano e si influenzano reciprocamente.
Staphylococcus epidermidis, batterio commensale abbondante sulla pelle, ha una funzione protettiva producendo sostanze antimicrobiche che contrastano i filotipi patogeni di C. acnes [5]. In campioni di cute sana, C. acnes e S. epidermidis coesistono armoniosamente all'interno di comunità batteriche eterogenee. Nel contesto dell'acne, invece, l'equilibrio si spezza: la diversità ceppo-specifica si riduce e l'abbondanza relativa di S. epidermidis aumenta in modo compensatorio.
L'infiammazione caratteristica dell'acne origina da un'attivazione immunitaria inappropriata. I filotipi virulenti di C. acnes producono fattori CAMP (Christie-Atkins-Munch-Petersen), tossine citotossiche che generano pori nella membrana cellulare e attivano l'infiammazione cutanea attraverso il riconoscimento dei recettori Toll-like di tipo 2 (TLR-2). La cascata infiammatoria induce la produzione di citochine proinfiammatorie, leucotriene B4 e prostaglandina E2, amplificando il processo infiammatorio caratteristico delle lesioni acneiche.
La capacità di formare biofilm da parte del filotipo IA1 costituisce un meccanismo di difesa particolarmente insidioso. Il biofilm - una matrice protettiva composta da polisaccaridi extracellulari - protegge i batteri dall'azione degli antibiotici e del sistema immunitario, spiegando la persistenza batterica cronica e le frequenti recidive dopo terapia antibiotica.
L'asse intestino-pelle
La comprensione dell'acne si è ulteriormente arricchita con la scoperta dell'asse intestino-cervello-pelle, una rete di comunicazione bidirezionale che collega il microbiota intestinale alla salute cutanea [6]. Stress psicologico, ansia e depressione possono alterare la composizione del microbiota intestinale, aumentare la permeabilità intestinale e contribuire all'infiammazione sistemica che si riflette sulla pelle.
Diversi studi hanno documentato differenze significative nel microbiota intestinale di pazienti con acne rispetto a controlli sani [7]. I soggetti con acne mostrano diversità ridotta del microbiota intestinale, con diminuzione dei phyla Firmicutes e aumento di Bacteroidetes - un enterotipo tipicamente associato alla dieta occidentale ricca di grassi saturi e zuccheri raffinati.
Specificamente, si osserva deplezione di Lactobacillus, Bifidobacterium, Butyricicoccus e altri produttori di acidi grassi a catena corta (SCFA), metaboliti benefici che regolano l'infiammazione sistemica.
Il meccanismo proposto coinvolge multiple vie: il microbiota intestinale alterato produce meno SCFA anti-infiammatori, aumenta la permeabilità intestinale permettendo il passaggio di endotossine batteriche nel circolo sanguigno, e altera l'asse ipotalamo-ipofisi-surrene modificando la risposta allo stress. L'asse IGF-1 (fattore di crescita insulino-simile) ha anch'esso una funzione determinante: diete ad alto indice glicemico e latticini stimolano la produzione di IGF-1, che a sua volta aumenta la produzione di sebo e l'infiammazione follicolare.
Oltre all'acne, moltissime patologie della pelle sono legate all'alimentazione, prima tra tutte la psoriasi. Per questo, gli scienziati e i dietologi hanno elaborato un una dieta anti-psoriasi. Si tratta di un protocollo alimentare equilibrato e bilanciato che sebbene non si proponga come una cura miracolosa, può aiutare nel tenere sotto controllo le alterazioni del microbioma cutaneo che scatenano acne, dermatiti, eczemi e psoriasi.
I trattamenti tradizionali sotto accusa
Gli approcci terapeutici convenzionali per l'acne - antibiotici topici e sistemici, perossido di benzoile, isotretinoina - mostrano efficacia clinica, sebbene il loro impatto sul microbioma cutaneo sollevi crescenti preoccupazioni [8].
Gli antibiotici causano danni collaterali estesi, inducendo resistenza antimicrobica e disregolazione dell'equilibrio microbico anche con cicli di breve durata. Il perossido di benzoile, pur non inducendo resistenza, elimina indiscriminatamente batteri benefici insieme a quelli patogeni.
L'isotretinoina orale - farmaco riservato ai casi gravi - modifica profondamente la fisiologia cutanea riducendo la produzione di sebo, sebbene il suo effetto sul microbioma rimanga controverso e richieda ulteriori approfondimenti.
La crescente resistenza antimicrobica di C. acnes agli antibiotici comunemente utilizzati (eritromicina, clindamicina, doxiciclina) costituisce una sfida clinica rilevante, spingendo la ricerca verso alternative non antibiotiche.
Le nuove frontiere terapeutiche
Il futuro del trattamento dell'acne si orienta verso strategie che preservano e ripristinano l'equilibrio microbico piuttosto che distruggerlo. I probiotici topici stanno emergendo in modo promettente: specifici ceppi di Lactobacillus e Bifidobacterium applicati sulla pelle possono competere con i filotipi patogeni di C. acnes, produrre sostanze antimicrobiche selettive e regolare la risposta infiammatoria locale.
I probiotici orali hanno mostrato risultati incoraggianti negli studi clinici, generando una risposta anti-infiammatoria sistemica, ripristinando l'integrità della barriera intestinale e regolando l'asse IGF-1 [9]. La fagoterapia - l'utilizzo di batteriofagi specifici che infettano selettivamente i ceppi patogeni di C. acnes risparmiando quelli benefici - è in fase di ricerca attiva. Alcuni studi hanno dimostrato che batteriofagi naturali di C. acnes sono più diffusi sulla pelle di individui sani rispetto a pazienti con acne.
L'ingegneria genetica del microbioma potrebbe costituire la vera rivoluzione: modificando specifici ceppi di C. acnes per renderli resistenti all'attacco dei fagi, si potrebbero propagare fagi che uccidono selettivamente i taxa inclini all'acne, lasciando intatti i ceppi probiotici. I postbiotici - metaboliti e componenti cellulari derivati da batteri benefici - offrono i vantaggi dei probiotici senza i rischi associati all'applicazione di microrganismi vivi.
Il supporto degli estratti botanici
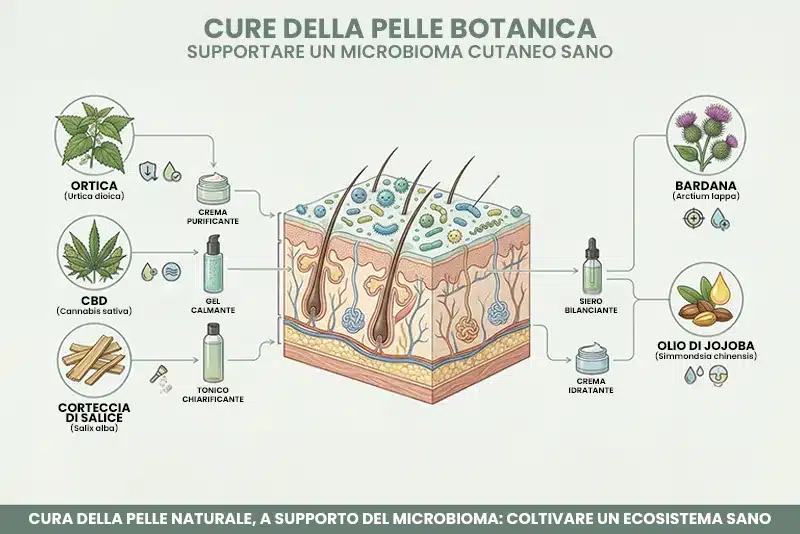
Parallelamente all'evoluzione della comprensione scientifica, anche la formulazione dei trattamenti topici sta evolvendo verso approcci più rispettosi del microbioma. Estratti botanici specifici hanno dimostrato capacità di regolare l'infiammazione e supportare l'equilibrio microbico senza gli effetti collaterali dei trattamenti convenzionali.
L'estratto di ortica (Urtica dioica) possiede proprietà seboregolatrici e anti-infiammatorie documentate, agendo sulla 5-alfa-reduttasi senza compromettere il microbioma. Il cannabidiolo (CBD) estratto dalla Cannabis sativa ha mostrato attività sebostatica sui sebociti umani, riducendo la produzione di sebo e regolando le vie infiammatorie attraverso l'interazione con il sistema endocannabinoide cutaneo. L'estratto di salice (Salix alba), fonte naturale di acido salicilico, offre azione cheratolitica delicata supportando il turnover cellulare senza alterare drasticamente il pH cutaneo. Tale meccanismo è stato approfondito nel nostro articolo dedicato a CBD e acne.
L'estratto di bardana (Arctium lappa) viene tradizionalmente utilizzato per le sue proprietà purificanti e antibatteriche selettive. L'olio di jojoba (Simmondsia chinensis), la cui composizione lipidica mima il sebo umano, può aiutare a bilanciare la produzione sebacea senza ostruire i pori. Alcuni prodotti innovativi combinano gli ingredienti botanici con CBD per un approccio sinergico: formulazioni quali creme viso al CBD specifiche per pelle acneica possono contenere ortica, salice, bardana e cannabidiolo in sinergia, offrendo un'alternativa naturale ai trattamenti aggressivi.
L'approccio completo richiede anche una detersione rispettosa del microbioma: detergenti delicati che mantengono il pH fisiologico senza eliminare indiscriminatamente i batteri benefici. Formulazioni di gel detergente per pelle acneica con estratti vegetali e pH bilanciato preparano la pelle ai trattamenti successivi senza compromettere l'ecosistema microbico. Trattamenti intensivi settimanali quali maschere viso purificanti con argilla e estratti botanici possono supportare il riequilibrio cutaneo senza danneggiare il microbioma.
Approccio integrato
La gestione moderna dell'acne richiede un approccio olistico che consideri tutti i fattori che influenzano il microbioma cutaneo e intestinale. Sul fronte alimentare, gli studi indicano benefici dalla riduzione di alimenti ad alto indice glicemico, limitazione di latticini, aumento del consumo di acidi grassi omega-3 (pesce, semi di lino), integrazione di alimenti fermentati ricchi di probiotici naturali, e consumo abbondante di fibre prebiotiche che nutrono il microbiota intestinale.
Lo stress cronico altera profondamente sia il microbiota intestinale che la risposta infiammatoria cutanea. Pratiche di gestione dello stress - meditazione, yoga, esercizio fisico regolare - possono contribuire indirettamente al miglioramento dell'acne attraverso la regolazione dell'asse intestino-cervello-pelle.
La routine di skincare deve rispettare il pH fisiologico della pelle (circa 5,5), utilizzare detergenti delicati che non distruggano il film idrolipidico, evitare lavaggi troppo frequenti che eliminano i batteri benefici, applicare prodotti che supportano la barriera cutanea, ed evitare l'uso indiscriminato di prodotti antibatterici aggressivi.
Una routine quotidiana efficace parte dalla detersione: scopri come detergere correttamente la pelle grassa senza compromettere il microbioma.
Diagnosi personalizzata
Il futuro della dermatologia vede l'analisi del microbioma cutaneo individuale diventare strumento diagnostico. Tecnologie di sequenziamento del DNA permetteranno di identificare il profilo microbico specifico di ogni paziente, determinando quali filotipi di C. acnes predominano, valutando la diversità complessiva del microbioma e identificando squilibri specifici. Sulla base di tale analisi, sarà possibile prescrivere trattamenti personalizzati: probiotici mirati, fagi specifici per i ceppi patogeni presenti, interventi dietetici cuciti sulle caratteristiche del microbiota intestinale.
L'intelligenza artificiale sta già supportando tale evoluzione, analizzando grandi database di profili microbici correlati a fenotipi clinicied evidenziando quali trattamenti saranno più efficaci per specifici profili di microbioma. Alcune app e dispositivi consentono già il monitoraggio del pH cutaneo e della produzione di sebo, parametri che riflettono indirettamente lo stato del microbioma.
Recap Generale
Il 2026 segna un punto di svolta nella comprensione e nel trattamento dell'acne. La transizione da un modello semplicistico basato sull'eliminazione batterica a un approccio ecologico basato sul ripristino dell'equilibrio microbico non è solo più raffinata scientificamente, bensì più efficace e sostenibile. La consapevolezza che C. acnes non è un nemico monolitico, in realtà una famiglia complessa di ceppi con funzioni diverse, ha aperto la strada a terapie mirate che preservano i batteri benefici eliminando selettivamente quelli patogeni.
L'asse intestino-pelle ci ricorda che la salute cutanea è inscindibilmente legata alla salute generale dell'organismo. Non possiamo più trattare l'acne ignorando l'influenza del microbiota intestinale, della dieta, dello stress e dello stile di vita. I trattamenti del futuro saranno personalizzati, rispettosi del microbioma e integrati in un approccio olistico che considera l'individuo nella sua totalità.
Mentre attendiamo l'arrivo delle terapie più innovative - probiotici di nuova generazione, fagoterapia, ingegneria del microbioma - possiamo già agire preservando e supportando il nostro ecosistema cutaneo attraverso scelte consapevoli in ambito di skincare, alimentazione e gestione dello stress. La rivoluzione del microbioma nell'acne non è solo scientifica: è culturale, invita a riconciliarci con i nostri invisibili coinquilini microbici e riconoscere in loro non nemici da annientare, bensì partner da coltivare per una pelle sana e in equilibrio.
Bibliografia
-
- [1] Pérez-Sánchez A, Barrajón-Catalán E, Herranz-López M, et al. Acne, Microbiome, and Probiotics: The Gut-Skin Axis. Microorganisms. 2022;10(7):1303;
-
- [2] Dall'Oglio F, Tedeschi A, Micali G, et al. The Role of the Skin Microbiome in Acne: Challenges and Future Therapeutic Opportunities. Life (Basel). 2024;14(11):1388;
-
- [3] Cutibacterium acnes: il batterio dell'acne. Microbiologia Italia. 2022;
-
- [4] Di Domenico EG, Cavallo I, Sivori F, et al. Individuato specifico ceppo di Cutibacterium acnes responsabile dell'acne. Scientific Reports. 2022;
-
- [5] O'Neill AM, Gallo RL. Acne e microbiota cutaneo: lo stato dell'arte della ricerca. Microbiome. 2024;
-
- [6] Deng Y, Wang H, Zhou J, Mou Y, Wang G, Xiong X. Potential Role of the Microbiome in Acne: A Comprehensive Review. J Clin Med. 2019;8(7):1050;
-
- [7] Li M, Chen Y, Wang X. The gut-skin axis: Emerging insights in understanding and treating skin diseases through gut microbiome modulation. Mol Med Rep. 2025;31(1);
-
- [8] Dessinioti C, Katsambas A. The Microbiome and Acne: Perspectives for Treatment. Dermatol Ther (Heidelb). 2024;14(1):31-44;
-
- [9] Bowe W, Patel NB, Logan AC. Acne vulgaris, probiotics and the gut-brain-skin axis: from anecdote to translational medicine. Benef Microbes. 2014;5(2):185-199.
Iscriviti alla nostra newsletter.
Scrivi un commento
Devi essere connesso per inviare un commento.